La bacteria klebsiella pneumoniae représente aujourd’hui un défi majeur pour la médecine moderne et la sécurité des soins. Ce bacille, souvent présent de manière inoffensive dans notre organisme, peut se transformer en un redoutable agent infectieux sous certaines conditions. Comprendre ses mécanismes de transmission, ses symptômes et ses résistances est essentiel pour protéger les populations vulnérables. Cet article détaille les aspects cliniques, biologiques et préventifs indispensables pour appréhender cette menace sanitaire avec professionnalisme et rigueur scientifique.
Comprendre la nature de la bacteria klebsiella pneumoniae
La bacteria klebsiella pneumoniae appartient à la vaste famille des Enterobacteriaceae. Il s’agit d’un micro-organisme ubiquitaire que l’on retrouve aussi bien dans l’environnement que chez l’humain. Dans le corps, elle colonise principalement le tube digestif et l’oropharynx sans provoquer de maladie initiale. Cependant, sa nature opportuniste signifie qu’elle profite de la moindre faille immunitaire pour envahir des sites normalement stériles.
Cette bactérie est particulièrement redoutée en milieu hospitalier pour sa capacité à survivre sur des surfaces inertes durant de longues périodes. Afin de mieux cerner ce pathogène, il convient d’étudier sa structure biologique unique ainsi que ses proches parents microbiologiques.
Morphologie et caractéristiques de k pneumoniae bacteria
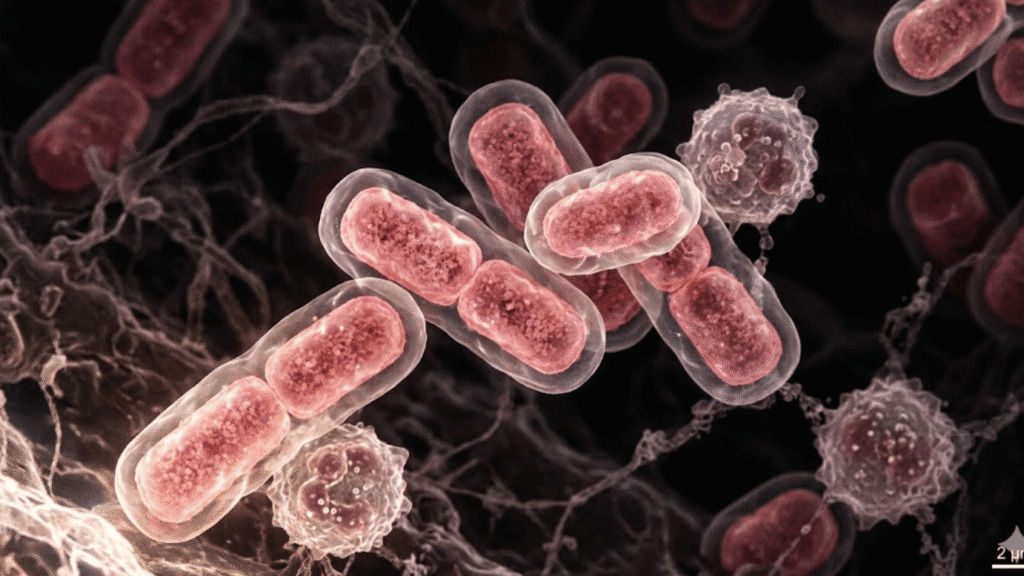
L’aspect visuel de k pneumoniae bacteria au microscope est très caractéristique. Ce sont des bâtonnets courts, à Gram négatif, qui ne possèdent pas de flagelles pour se déplacer. Leur trait le plus distinctif reste une épaisse capsule composée de polysaccharides complexes.
Cette enveloppe protectrice agit comme un véritable bouclier contre les attaques du système immunitaire de l’hôte. Elle empêche notamment les globules blancs de détruire efficacement la bactérie par phagocytose. En laboratoire, cette capsule donne aux colonies un aspect gluant ou muqueux très reconnaissable sur les boîtes de culture.
Distinction avec la bacteria klebsiella oxytoca
Il arrive fréquemment que l’on confonde cette espèce avec la bacteria klebsiella oxytoca. Bien que ces deux micro-organismes partagent un patrimoine génétique proche, ils présentent des différences métaboliques notables. La principale distinction repose sur le test de l’indole, qui est positif pour l’espèce oxytoca et négatif pour pneumoniae.
Sur le plan clinique, la bacteria klebsiella oxytoca est également impliquée dans des infections nosocomiales, mais elle est plus spécifiquement liée à des colites hémorragiques post-antibiotiques. Identifier précisément l’espèce est crucial pour adapter le suivi épidémiologique et comprendre l’origine d’un foyer infectieux.
Les différents types et souches de kleb pneumo
Le genre Klebsiella n’est pas monolithique et présente une grande hétérogénéité génétique. Les chercheurs classent généralement les isolats de kleb pneumo en fonction de leur virulence et de leur profil de résistance. Cette classification est indispensable pour évaluer le pronostic vital du patient et choisir la stratégie thérapeutique la plus efficace.
On observe depuis quelques années une scission inquiétante entre les souches classiques et les nouvelles variantes hypervirulentes. L’étude de ces souches repose sur des critères moléculaires et sérologiques précis qui permettent de tracer la propagation de la bactérie à l’échelle mondiale.
Classification sérologique et capsulaire
La diversité de la bacteria klebsiella pneumoniae s’exprime à travers ses antigènes de surface. On distingue l’antigène O, situé sur le lipopolysaccharide, et l’antigène K, propre à la capsule. Il existe actuellement plus de 80 types capsulaires recensés. Certains sérotypes, comme le K1 et le K2, sont historiquement associés à des infections plus sévères et à une plus grande capacité de dissémination hématogène. Cette caractérisation permet aux épidémiologistes de surveiller l’émergence de clones particulièrement agressifs au sein d’une structure hospitalière ou d’une région géographique donnée.
Émergence des souches multirésistantes
Le problème majeur de kleb pneumo réside dans son incroyable plasticité génétique. La bactérie acquiert facilement des plasmides contenant des gènes de résistance aux antibiotiques. Les souches productrices de carbapénémases sont les plus préoccupantes, car elles neutralisent presque toutes les options de traitement disponibles.
Ces « super-bactéries » ne sont plus seulement l’apanage des hôpitaux et commencent à circuler dans la communauté. Cette évolution oblige les autorités de santé à renforcer les mesures de contrôle pour limiter l’impasse thérapeutique qui menace les patients infectés.
Modes de transmission et personnes à risques
La propagation de la bacteria klebsiella pneumoniae obéit à des règles strictes de contact. Contrairement à certains virus respiratoires, cette bactérie ne voyage pas sur de longues distances par de fines gouttelettes suspendues dans l’air. Son mode de transmission principal reste le contact direct, souvent par l’intermédiaire des mains.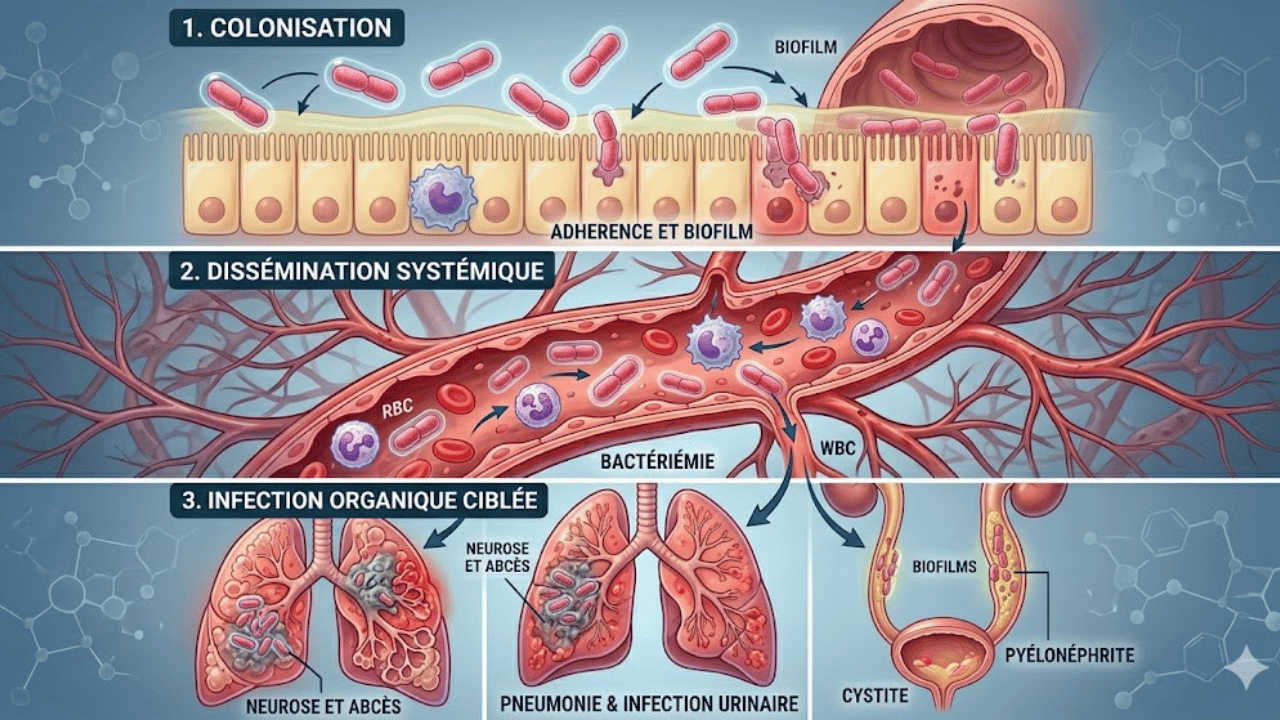
Un environnement contaminé ou un matériel médical mal désinfecté peut également servir de réservoir. Cette caractéristique explique pourquoi la gestion de l’hygiène est le pilier central de la lutte contre ce pathogène en milieu clinique. Pour mieux comprendre comment cette bactérie s’installe, il faut examiner les vecteurs de propagation et les terrains fragiles qu’elle affectionne.
Les vecteurs de propagation en milieu hospitalier
En milieu de soins, les surfaces inertes jouent un rôle crucial. La bacteria klebsiella pneumoniae peut survivre sur des poignées de porte, des barrières de lit ou des claviers d’ordinateur. Le personnel soignant, en passant d’un patient à l’autre, peut transporter la bactérie si le lavage des mains est omis.
L’utilisation de dispositifs invasifs, tels que les sondes urinaires ou les tubes d’intubation, facilite également l’entrée du micro-organisme dans des zones normalement protégées. La formation continue des équipes médicales est donc vitale pour briser cette chaîne de contamination.
Qui sont les individus les plus vulnérables ?
Tout le monde n’est pas égal face à une exposition à la bacteria klebsiella pneumoniae. Le système immunitaire joue un rôle de rempart naturel que la bactérie tente de contourner. Certains profils présentent un risque accru de développer une forme grave de l’infection :
- Les patients souffrant de pathologies chroniques comme le diabète ou l’insuffisance rénale.
- Les personnes âgées dont les défenses immunitaires sont naturellement plus affaiblies.
- Les nouveau-nés prématurés en unités de soins intensifs néonatals.
- Les individus ayant subi une antibiothérapie prolongée, ce qui déséquilibre leur flore protectrice.
Symptômes et manifestations cliniques de l’infection
L’expression clinique d’une infection à bacteria klebsiella pneumoniae dépend fortement du site de colonisation primaire. La bactérie est capable d’attaquer plusieurs organes, provoquant des tableaux cliniques variés. Le diagnostic précoce repose souvent sur l’observation de signes spécifiques qui alertent le personnel médical.
Une prise en charge rapide est nécessaire pour éviter que l’infection ne se propage de manière systémique à l’ensemble de l’organisme. Le spectre des maladies engendrées par ce pathogène est large, allant de la simple infection locale à la détresse respiratoire majeure.
Signes d’une infection pulmonaire aiguë
La pneumonie causée par la bacteria klebsiella pneumoniae est souvent brutale. Elle se manifeste par une fièvre élevée accompagnée de frissons intenses. Un signe clinique classique, bien que non systématique, est l’émission de crachats gélatineux de couleur groseille. Le patient ressent une difficulté respiratoire marquée, souvent liée à une inflammation sévère des tissus pulmonaires. Dans les cas les plus graves, la bactérie provoque une nécrose du parenchyme, entraînant la formation d’abcès visibles à la radiographie thoracique.
Présence de klebsiella pneumoniae dans l’urine
Lorsqu’on détecte le klebsiella pneumoniae dans l’urine, le tableau clinique ressemble à celui d’une cystite bactérienne classique. Le patient rapporte des douleurs ou des brûlures lors de la miction. L’urine peut apparaître trouble ou présenter des traces de sang.
Si la bactérie remonte vers les uretères, elle peut causer une pyélonéphrite aiguë, caractérisée par des douleurs lombaires et une altération de l’état général. Cette situation nécessite une surveillance accrue, car les voies urinaires constituent une porte d’entrée fréquente pour une infection généralisée du sang.
Lire aussi : Taux de bilirubine et cancer : quand faut-il s’inquiéter ?
Diagnostic et mise en évidence de la bacteria klebsiella pneumoniae
L’identification précise de la bacteria klebsiella pneumoniae est une étape fondamentale du protocole médical. Les médecins ne peuvent pas se baser uniquement sur les symptômes, car ceux-ci ressemblent à d’autres infections bactériennes. Le laboratoire de microbiologie devient alors le partenaire indispensable du clinicien.
La rapidité du diagnostic influence directement le choix thérapeutique et les mesures d’isolement à mettre en place pour protéger les autres patients. Le processus diagnostique suit un protocole rigoureux, allant du prélèvement biologique à l’analyse fine de la sensibilité aux traitements.
| Type de Prélèvement | Objectif du Diagnostic | Méthode d’Analyse |
| Hémoculture | Détecter une septicémie | Mise en culture aérobie/anaérobie |
| ECBU | Analyser klebsiella pneumoniae dans l’urine | Numération et antibiogramme |
| Prélèvement distal | Identifier une pneumonie | Culture et examen direct |
Techniques de laboratoire et culture
Une fois le prélèvement reçu, les techniciens procèdent à un examen direct sous microscope après une coloration de Gram. La présence de bacilles Gram négatif est un premier indice sérieux. Ensuite, l’échantillon est ensemencé sur des milieux de culture spécifiques. La bacteria klebsiella pneumoniae se développe rapidement en formant des colonies bombées et brillantes. L’utilisation de la technologie MALDI-TOF permet aujourd’hui d’identifier l’espèce avec une précision extrême en quelques minutes seulement après la croissance initiale.
L’importance cruciale de l’antibiogramme
La simple identification de l’espèce ne suffit plus à notre époque. Il est vital de réaliser un antibiogramme pour connaître le profil de résistance de la souche isolée. Ce test consiste à exposer la bactérie à différents antibiotiques pour observer son inhibition ou sa croissance. En raison de la capacité de la bacteria klebsiella pneumoniae à produire des enzymes neutralisantes, ce test guide le médecin vers la molécule la plus efficace. Sans cette étape, le risque d’échec thérapeutique et de complications graves augmente considérablement pour le patient.
Complications et risques à long terme
Une infection par la bacteria klebsiella pneumoniae ne doit jamais être prise à la légère. Si le traitement est retardé ou inadapté, la bactérie peut causer des dommages irréversibles aux tissus qu’elle colonise. La capacité de ce pathogène à former des abcès profonds constitue l’une de ses complications les plus redoutables.
Ces poches de pus, remplies de bactéries et de débris cellulaires, sont particulièrement difficiles à drainer et à traiter par les seuls antibiotiques. Le passage de la bactérie dans la circulation générale marque souvent un tournant critique dans l’évolution de la maladie.
Le choc septique et la défaillance multiviscérale
La septicémie survient lorsque la bacteria klebsiella pneumoniae envahit le sang. Ce phénomène déclenche une réponse inflammatoire généralisée et disproportionnée de l’organisme. Le patient peut alors entrer en choc septique, une urgence absolue caractérisée par une chute brutale de la tension artérielle.
Les organes vitaux, comme les reins et le foie, cessent de fonctionner correctement faute d’une irrigation sanguine suffisante. Une prise en charge en unité de réanimation est alors impérative pour soutenir les fonctions vitales et tenter d’éradiquer l’infection.
Klebsiella pneumoniae et le risque de cancer
La recherche scientifique s’intéresse de plus près au lien entre klebsiella pneumoniae et le risque de cancer, particulièrement au niveau du côlon. Certaines souches possèdent un gène capable de synthétiser une toxine appelée colibactine. Cette substance peut provoquer des cassures dans l’ADN des cellules intestinales de l’hôte.
À long terme, ces dommages génétiques non réparés peuvent favoriser l’apparition de mutations cancéreuses. Bien que les études soient encore en cours, cette piste souligne l’importance de surveiller l’équilibre du microbiote intestinal.
Traitements et gestion de la résistance aux antibiotiques
Le traitement de la bacteria klebsiella pneumoniae est devenu un défi quotidien pour les infectiologues. Cette bactérie possède une résistance naturelle à certaines familles d’antibiotiques, comme les aminopénicillines. Cependant, c’est sa capacité à acquérir de nouvelles résistances qui inquiète la communauté internationale.
L’utilisation massive d’antibiotiques a sélectionné des souches capables de survivre aux traitements de dernier recours. La stratégie thérapeutique doit donc être à la fois rapide et extrêmement précise pour espérer un succès clinique.
Stratégies thérapeutiques actuelles
Pour une infection simple, le médecin s’appuie sur l’antibiogramme pour prescrire la molécule la plus adaptée. On utilise fréquemment des céphalosporines de troisième génération ou des fluoroquinolones. Cependant, si la bacteria klebsiella pneumoniae est identifiée comme productrice de BLSE, le choix se restreint considérablement. Dans ces situations, les carbapénèmes deviennent souvent le pivot du traitement. Le respect des doses et de la durée du traitement est fondamental pour éviter l’émergence de nouvelles résistances au sein de la flore du patient.
Le défi des souches productrices de carbapénémases
L’apparition de la bacteria klebsiella pneumoniae résistante aux carbapénèmes (KPC) représente une impasse thérapeutique majeure. Ces bactéries sont capables de dégrader les antibiotiques les plus puissants de notre arsenal. Les médecins sont alors contraints d’utiliser des molécules plus anciennes, parfois plus toxiques, ou des combinaisons d’antibiotiques expérimentales. La gestion de ces patients nécessite un isolement strict en chambre individuelle. Cette situation illustre parfaitement la nécessité d’une gestion raisonnée des antibiotiques à l’échelle mondiale.
Prévention et mesures d’hygiène
La prévention reste l’arme la plus efficace contre la bacteria klebsiella pneumoniae. Puisque la bactérie se transmet principalement par les mains, l’hygiène manuelle est la première barrière de protection. En milieu hospitalier, des protocoles rigoureux sont mis en place pour limiter la diffusion de la bactérie d’un patient à un autre.
Ces mesures ne sont pas seulement l’affaire des soignants, mais concernent également les visiteurs et les patients eux-mêmes. Une prévention réussie repose sur une combinaison de gestes simples et de procédures techniques spécialisées.
Protocoles d’hygiène en milieu de soins
Les établissements de santé appliquent des précautions standard pour chaque patient. En présence de bacteria klebsiella pneumoniae multirésistante, des précautions complémentaires de type « contact » sont instaurées. Cela implique :
- Le port systématique d’une surblouse à usage unique et de gants pour tout soin.
- Une friction hydroalcoolique des mains avant et après chaque contact.
- Le bionettoyage quotidien des surfaces avec des produits détergents-désinfectants homologués.
- L’utilisation de matériel médical dédié uniquement au patient porteur de la bactérie.
Conseils pour les patients à domicile
Pour les personnes fragiles vivant à domicile, la vigilance doit être constante. Il est conseillé de nettoyer régulièrement les zones de contact fréquent, comme les téléphones ou les télécommandes. Une alimentation équilibrée et une bonne hydratation aident également à maintenir des barrières muqueuses efficaces. En cas de soins à domicile, comme le changement d’un pansement ou d’une sonde, le lavage des mains doit être scrupuleux. Ces gestes du quotidien réduisent significativement le risque que la bacteria klebsiella pneumoniae ne devienne pathogène.
Le klebsiella pneumoniae dans l’urine : est-ce grave ?
La découverte de klebsiella pneumoniae dans l’urine lors d’un examen de routine ou suite à des symptômes est une situation fréquente en urologie. La gravité de cette présence dépend avant tout du terrain du patient et de la souche bactérienne en cause. Dans de nombreux cas, la bactérie peut simplement coloniser la vessie sans provoquer de lésions immédiates, mais elle nécessite une surveillance étroite pour éviter toute ascension vers les reins. Il est essentiel de différencier les simples colonisations des infections actives qui menacent l’équilibre de l’appareil urinaire.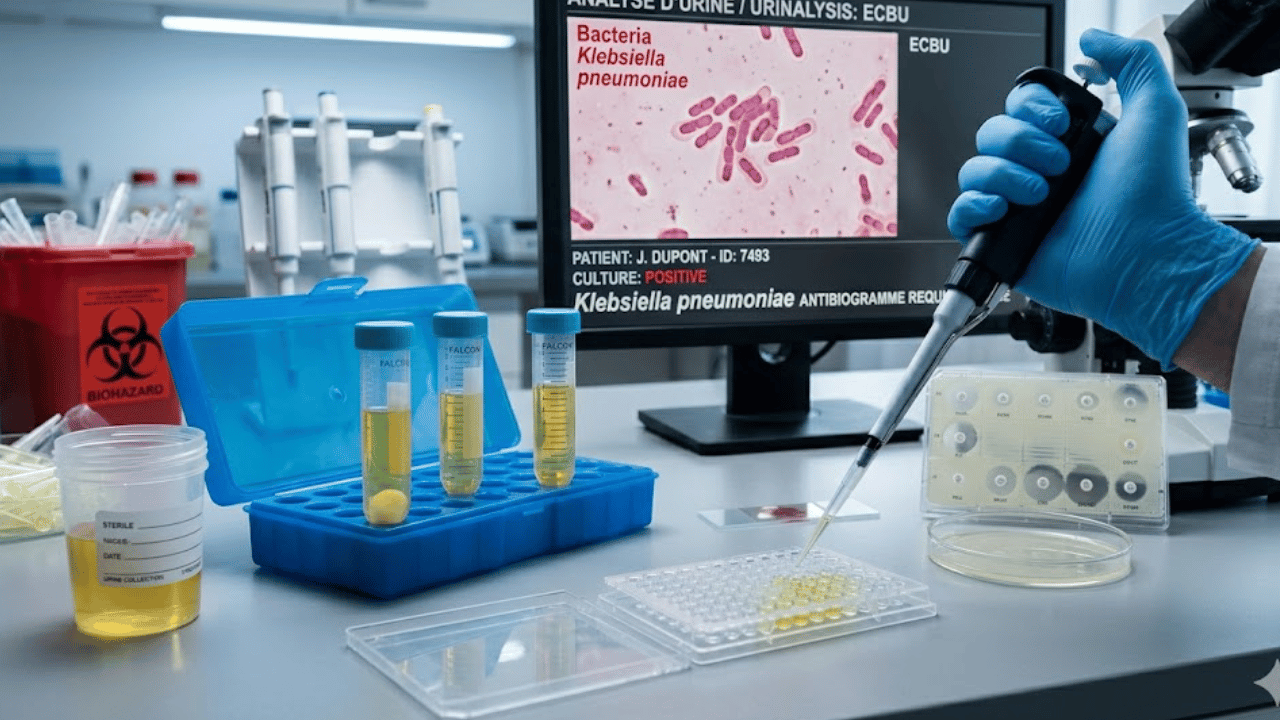
Infection versus colonisation
Une distinction fondamentale doit être faite entre la bactériurie asymptomatique et l’infection urinaire. Si l’on trouve klebsiella pneumoniae dans l’urine sans aucun symptôme associé (pas de douleur, pas de fièvre), on parle de colonisation. Chez les personnes âgées ou les porteurs de sondes urinaires, cette situation est courante et ne justifie pas toujours un traitement antibiotique. En revanche, si des signes inflammatoires apparaissent, la bactérie est considérée comme pathogène et doit être éradiquée pour prévenir des lésions tissulaires plus profondes.
Risque de pyélonéphrite et de récidive
La bacteria klebsiella pneumoniae possède des adhésines, de petites structures qui lui permettent de s’agripper fermement aux parois de l’urètre et de la vessie. Si l’infection n’est pas traitée, la bactérie remonte vers les uretères jusqu’aux reins, provoquant une pyélonéphrite aiguë.
Cette complication est grave car elle peut endommager les néphrons et conduire à une septicémie. De plus, cette bactérie est connue pour sa capacité à former des biofilms sur le matériel médical, ce qui explique pourquoi les infections urinaires à Klebsiella sont souvent récidivantes et difficiles à éliminer définitivement.
FAQ sur la bacteria klebsiella pneumoniae
Comment savoir si je suis porteur de la bactérie ?
Le portage sain est fréquent au niveau de l’intestin. Pour savoir si vous développez une infection, un médecin prescrira des analyses biologiques comme un ECBU pour les urines ou une hémoculture pour le sang. Seul un test de laboratoire peut confirmer la présence de la bacteria klebsiella pneumoniae.
Pourquoi est-elle résistante aux antibiotiques ?
Cette bactérie possède des mécanismes génétiques lui permettant de produire des enzymes, comme les carbapénémases, qui détruisent les antibiotiques avant qu’ils n’agissent. Elle peut également modifier sa paroi pour empêcher l’entrée des médicaments. Cette résistance est renforcée par l’usage excessif ou inapproprié des traitements antibiotiques.
Peut-on attraper klebsiella pneumoniae au restaurant ?
C’est extrêmement rare. Bien que la bactérie puisse se trouver sur certains aliments crus mal lavés, elle est principalement un pathogène hospitalier. La transmission alimentaire n’est pas la voie principale de contamination, contrairement à d’autres bactéries comme la Salmonella.
Quel est le lien entre klebsiella pneumoniae et le cancer ?
Des études suggèrent que certaines souches produisent de la colibactine, une toxine qui endommage l’ADN des cellules du côlon. Ce processus inflammatoire chronique pourrait, sur plusieurs années, augmenter la probabilité de développer des tumeurs colorectales. La recherche continue d’explorer ce lien complexe pour mieux prévenir ces risques.